肺癌临床试验新型免疫疗法——替瑞利尤单抗获FDA突破性疗法认定
众所周知,肺癌是全球最常见的恶性肿瘤之一,已成为我国城市人口恶性肿瘤死亡原因的第1位。每年约有160万人因肺癌而死亡,其中大约85%的肺癌患者的肿瘤组织学亚型为非小细胞肺癌。
从最初的细胞毒性化疗到靶向治疗,再到现在的免疫治疗,非小细胞肺癌的治疗取得了重大的进展。
2021年1月5日,罗氏旗下基因泰克宣布,其靶向TIGIT的新型癌症免疫疗法替瑞利尤单抗(Tiragolumab)获得美国食品药品监督管理局(FDA)授予的突破性疗法认定,拟用于联合阿替利珠单抗拟用于PD-L1高表达、无EGFR或ALK基因组肿瘤突变的转移性非小细胞肺癌患者的一线治疗。
据悉,替瑞利尤单抗是第一个获得FDA批准突破性疗法认定的抗TIGIT分子,基于II期CITYSCAPE试验的随机数据,在高水平PD-L1(肿瘤比例评分TPS≥50%)人群中开展的探索性分析显示,替瑞利尤单抗和阿替利珠单抗联合治疗,同时阻断靶向免疫抑制受体TIGIT和PD-L1,有可能通过增强机体对癌细胞的免疫反应来增加抗肿瘤活性。与阿替利珠单抗单药治疗相比,明显获益。
从最初的细胞毒性化疗到靶向治疗,再到现在的免疫治疗,非小细胞肺癌的治疗取得了重大的进展。
2021年1月5日,罗氏旗下基因泰克宣布,其靶向TIGIT的新型癌症免疫疗法替瑞利尤单抗(Tiragolumab)获得美国食品药品监督管理局(FDA)授予的突破性疗法认定,拟用于联合阿替利珠单抗拟用于PD-L1高表达、无EGFR或ALK基因组肿瘤突变的转移性非小细胞肺癌患者的一线治疗。
据悉,替瑞利尤单抗是第一个获得FDA批准突破性疗法认定的抗TIGIT分子,基于II期CITYSCAPE试验的随机数据,在高水平PD-L1(肿瘤比例评分TPS≥50%)人群中开展的探索性分析显示,替瑞利尤单抗和阿替利珠单抗联合治疗,同时阻断靶向免疫抑制受体TIGIT和PD-L1,有可能通过增强机体对癌细胞的免疫反应来增加抗肿瘤活性。与阿替利珠单抗单药治疗相比,明显获益。
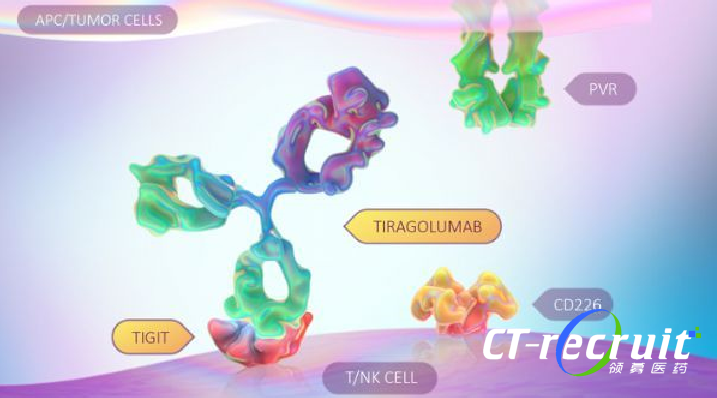
TIGIT(T细胞免疫球蛋白和TIIM 结构域)是新兴的 NK 细胞和 T 细胞共有的抑制性受体,可与肿瘤细胞上高表达的 PVR 受体相互结合,介导免疫反应的抑制信号,从而直接抑制 NK 细胞和 T 细胞对肿瘤细胞的杀伤作用,效果类似于 PD-1 对 T 细胞的抑制作用。
CITYSCAPE是TIGIT领域的首个随机研究,这是一项全球性、随机、双盲研究,在135例PD-L1阳性、局部晚期不可切除性或转移性NSCLC患者中开展,评估了阿替利珠单抗与替瑞利尤单抗联合疗法、阿替利珠单抗单药疗法用于初始(一线)治疗的疗效和安全性。该研究的共同主要终点是总缓解率和无进展生存期,次要终点包括安全性和总生存期。
在2020年美国临床肿瘤学会(ASCO)年会上公布的CITYSCAPE的完整结果显示:
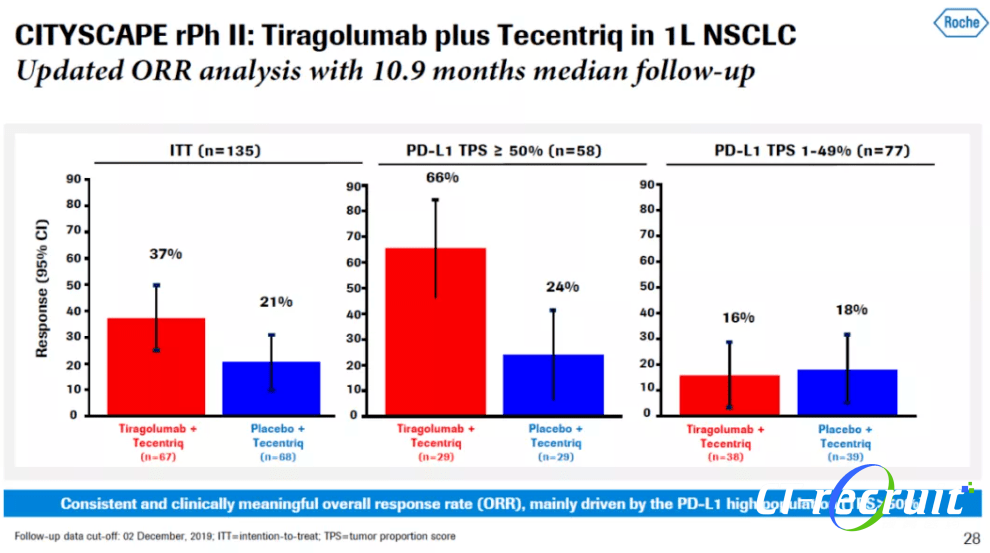
1、中位随访10.9个月,在意向性治疗患者群体中,与阿替利珠单抗单药治疗相比,阿替利珠单抗+替瑞利尤单抗联合治疗同时达到了2个主要终点:总缓解率显著提高(37% vs 21%)、疾病恶化或死亡风险显著降低42%(中位无进展生存期:5.6个月 vs 3.9个月;HR=0.58)。
2、对PD-L1高表达(TPS≥50%)患者开展的一项探索性分析显示:与阿替利珠单抗单药治疗相比,阿替利珠单抗+替瑞利尤单抗联合治疗显著提高总缓解率(66% vs 24%)、将疾病恶化或死亡风险显著降低70%(中位无进展生存期:未达到 vs 4.11个月;HR=0.30,95%CI:0.15-0.61)。
该研究中,阿替利珠单抗与替瑞利尤单抗联合治疗具有良好的耐受性,所有3级或以上全因不良事件的发生率方面,联合治疗与阿替利珠单抗单药治疗相似(48% vs 44%)。
CITYSCAPE是TIGIT领域的首个随机研究,这是一项全球性、随机、双盲研究,在135例PD-L1阳性、局部晚期不可切除性或转移性NSCLC患者中开展,评估了阿替利珠单抗与替瑞利尤单抗联合疗法、阿替利珠单抗单药疗法用于初始(一线)治疗的疗效和安全性。该研究的共同主要终点是总缓解率和无进展生存期,次要终点包括安全性和总生存期。
在2020年美国临床肿瘤学会(ASCO)年会上公布的CITYSCAPE的完整结果显示:
1、中位随访10.9个月,在意向性治疗患者群体中,与阿替利珠单抗单药治疗相比,阿替利珠单抗+替瑞利尤单抗联合治疗同时达到了2个主要终点:总缓解率显著提高(37% vs 21%)、疾病恶化或死亡风险显著降低42%(中位无进展生存期:5.6个月 vs 3.9个月;HR=0.58)。
2、对PD-L1高表达(TPS≥50%)患者开展的一项探索性分析显示:与阿替利珠单抗单药治疗相比,阿替利珠单抗+替瑞利尤单抗联合治疗显著提高总缓解率(66% vs 24%)、将疾病恶化或死亡风险显著降低70%(中位无进展生存期:未达到 vs 4.11个月;HR=0.30,95%CI:0.15-0.61)。
该研究中,阿替利珠单抗与替瑞利尤单抗联合治疗具有良好的耐受性,所有3级或以上全因不良事件的发生率方面,联合治疗与阿替利珠单抗单药治疗相似(48% vs 44%)。
这是令人振奋的消息,CITYSCAPE研究提供了第一个证据,即靶向免疫抑制受体TIGIT和PD-L1联合治疗,可以通过潜在地放大免疫反应来增强抗肿瘤活性。两者结合是一种有前途的抗癌治疗策略,有望增加患者对免疫治疗的反应,扩大可能受益人群的范围。
替瑞利尤单抗无疑已经迎来高光时刻,在 TIGIT 单抗版图的入场竞速中,罗氏、美施贵宝、默沙东等全球 Top 级肿瘤免疫霸主全部入局;百济神州、信达生物、君实生物、恒瑞医药等国内 Top 级肿瘤免疫企业也已全部入局。TIGIT 单抗药可能成为继在 PD-1 /PD-L1之后的首个通过 Ⅲ 期临床试验验证的新一代免疫疗法。
替瑞利尤单抗在国内上市只是时间问题,但是肿瘤患者的治疗刻不容缓,目前国内也有针对不同癌肿开展的临床试验项目,比如免疫治疗PD-1;PD-L1和TGF-β双靶生物药;抗PD-1/CD47双特异性抗体;免疫治疗PD-1联合EGFR单克隆抗体注射液;溶瘤病毒+伊立替康;CAR-T细胞疗法;多纳非尼联合PD-1/CLTA-4免疫双抗等,肿瘤复发找领募,有意向的病友可以拨打领募医药官方热线400-699-8889
罗曼罗兰说过的,这个世上只有一种真正的英雄主义,那就是,认清生活的真相,并且仍然热爱它。希望肿瘤患者在抗癌路上,多一点希望,少一丝无奈!
替瑞利尤单抗无疑已经迎来高光时刻,在 TIGIT 单抗版图的入场竞速中,罗氏、美施贵宝、默沙东等全球 Top 级肿瘤免疫霸主全部入局;百济神州、信达生物、君实生物、恒瑞医药等国内 Top 级肿瘤免疫企业也已全部入局。TIGIT 单抗药可能成为继在 PD-1 /PD-L1之后的首个通过 Ⅲ 期临床试验验证的新一代免疫疗法。
替瑞利尤单抗在国内上市只是时间问题,但是肿瘤患者的治疗刻不容缓,目前国内也有针对不同癌肿开展的临床试验项目,比如免疫治疗PD-1;PD-L1和TGF-β双靶生物药;抗PD-1/CD47双特异性抗体;免疫治疗PD-1联合EGFR单克隆抗体注射液;溶瘤病毒+伊立替康;CAR-T细胞疗法;多纳非尼联合PD-1/CLTA-4免疫双抗等,肿瘤复发找领募,有意向的病友可以拨打领募医药官方热线400-699-8889
罗曼罗兰说过的,这个世上只有一种真正的英雄主义,那就是,认清生活的真相,并且仍然热爱它。希望肿瘤患者在抗癌路上,多一点希望,少一丝无奈!